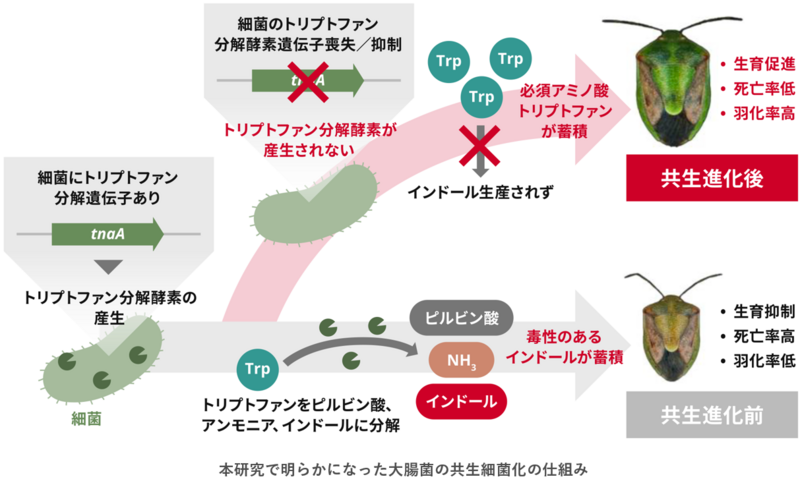
トリプトファン分解酵素が壊れると大腸菌はカメムシ共生細菌になる
ポイント
・ トリプトファン分解酵素の機能喪失で大腸菌および近縁の細菌がカメムシ共生細菌になることを実証
・ 自然界のカメムシ共生細菌で当該酵素遺伝子が失われていることを発見、共生進化への関与を示唆
・ 研究室における進化実験と野外生物集団の調査を統合し、共生進化に重要な分子基盤の一端を解明
概 要
国立研究開発法人産業技術総合研究所(以下「産総研」という)モレキュラーバイオシステム研究部門 バイオシステム多様性研究グループの汪 亜運 産総研特別研究員、森山 実 主任研究員、古賀 隆一 上級主任研究員、深津 武馬 首席研究員は、独自に開発したチャバネアオカメムシ-大腸菌実験共生進化系を駆使して、単一の酵素遺伝子(トリプトファン分解酵素)の機能喪失のみで、大腸菌がカメムシの腸内に共生して成長および生存を支える共生細菌に変化することを発見しました。トリプトファン分解酵素の喪失は、必須アミノ酸であるトリプトファンの濃度上昇、ならびに当該酵素の代謝産物として生成する毒性のあるインドールの濃度低下により、宿主カメムシの生育を改善することを示しました。さらに自然界に存在する多様なカメムシ類の生存を支持する能力を持つ腸内共生細菌のゲノムを調べたところ、トリプトファン分解酵素遺伝子を喪失していることが判明しました。そのような細菌にトリプトファン分解酵素遺伝子を導入して発現させるとカメムシに共生して成長と生存を支える能力(共生能力)が低下すること、またそれらの細菌とごく近縁でトリプトファン分解酵素遺伝子を持つ細菌から当該遺伝子を除去すると共生能力が向上することを示しました。すなわち、細菌におけるトリプトファン分解酵素の喪失が、研究室における実験共生進化のみならず、自然界のカメムシ類における共生進化でも重要な役割を果たしてきたことを明らかにしました。
本研究により、カメムシという昆虫類において、腸内細菌における単一酵素遺伝子の喪失が共生進化の鍵となりうることが判明し、共生進化が単一の突然変異で起こり得ること、またその分子機構および代謝基盤の一端が解明されました。共生進化の仕組みと過程を具体的に明らかにすることに成功した重要な成果です。
なお、本研究成果の詳細は2026年2月27日(英国時間)に国際学術誌「Nature Microbiology」にオンライ
ン掲載されます。
下線部は【用語解説】参照
開発の社会的背景
⽣態系の中で、多種多様な生物は単独で生きているのではなく、しばしば共生関係を構築して、それぞれの⽣息環境に適応しています。例えば、陸上生態系における生物多様性の中核をなす動物群である昆虫類には、広く微生物との密接な共生関係が見られ、共生微生物が宿主の生存や成長、機能に影響を及ぼすことが知られています。医学分野でも、ヒトの腸内細菌叢が消化器の生理状態や疾病のみならず、体質からメンタルに至るさまざまな健康状況に影響を与えることが判明し、大きな注目を集めています。このような背景のもと、生物多様性を基盤とする新規生物機能の解明と利用という観点から、腸内共生細菌には近年高い関心が寄せられており、盛んに研究開発が行われています。
研究の経緯
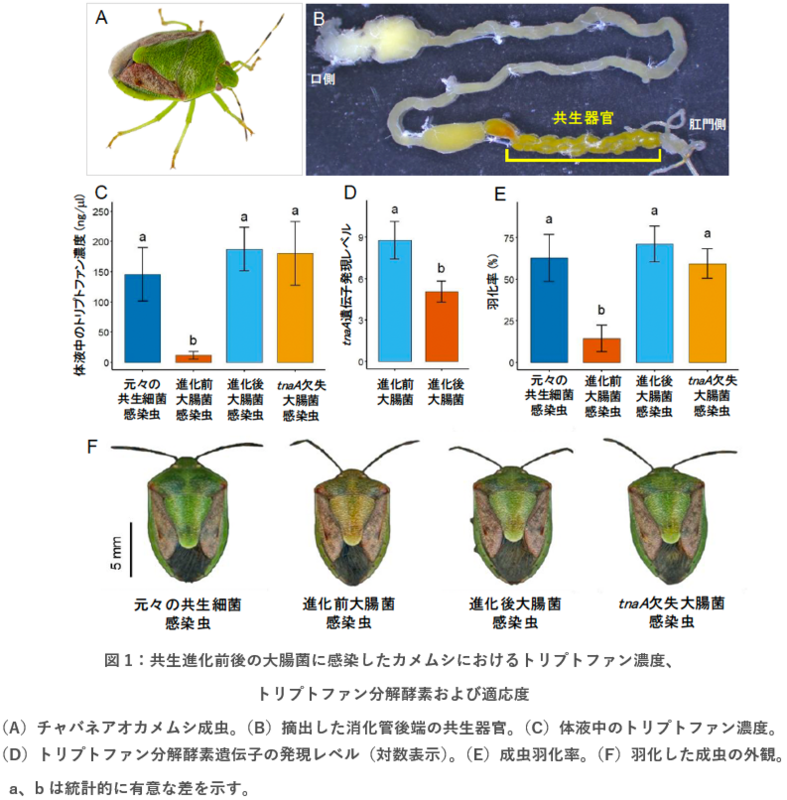
カメムシ類は世界に40,000種以上、⽇本に1,500種以上が分布しており、多くの農業害⾍が含まれます。近年は「カメムシ大発生」のニュースがしばしば報道されるなど、社会的にも大きな問題になっています。カメムシ類の多くは消化管に共生器官が発達しており、生存や成長に重要な役割を果たす共生細菌を保有しています(図1A、B)。産総研ではカメムシ類における共生細菌の新規機能の解明に取り組み、共生細菌による害虫化の発見(2007年6月13日 産総研プレス発表)、共生細菌による農薬耐性の発見(2012年4月24日 産総研プレス発表)、共生細菌の伝達に必須な宿主タンパク質の発見(2021年6月15日 産総研プレス発表)、後脚で培養した菌で寄生蜂から卵を守る防衛共生の発見(2025年10月17日産総研プレス発表)などの研究成果を挙げてきました。近年はチャバネアオカメムシを用いた昆虫-大腸菌実験共生進化系の開発に成功し(2022年8月5日 産総研プレス発表)、共生進化の過程や機構の理解に向けて、独創的なアプローチからの研究を展開しています。今回、この昆虫-大腸菌実験共生進化系を利用して、共生進化の鍵となる細菌遺伝子の同定に成功しました。
なお、本研究開発は、国⽴研究開発法⼈科学技術振興機構(JST)「ERATO 深津共⽣進化機構プロジェクト(JPMJER1902)」および科研費(新学術領域研究等)による⽀援を受けています。
研究の内容
昆虫-大腸菌実験共生進化系により作出された共生進化前の大腸菌、共生進化後の大腸菌をそれぞれカメムシに感染させ、体内の代謝産物や遺伝子発現を比較したところ、共生進化後の大腸菌に感染したカメムシでは必須アミノ酸の一つであるトリプトファンの体内濃度が著しく上昇していました(図1C)。共生進化前後の大腸菌で発現量が有意に変動した遺伝子を探索したところ、トリプトファン分解酵素遺伝子の発現量が顕著に低下していました(図1D)。そこでトリプトファン分解酵素遺伝子を欠失させた大腸菌をカメムシに感染させてみたところ、トリプトファンの体内濃度が進化後の大腸菌や元々の共生細菌に感染したカメムシと同等のレベルまで上昇し(図1C)、羽化率(図1E)や体色(図1F)が顕著に改善しました。すなわち、トリプトファン分解酵素遺伝子の機能喪失によって、必須アミノ酸であるトリプトファンの体内濃度が上昇し、大腸菌の共生細菌化に寄与する可能性が示されました。
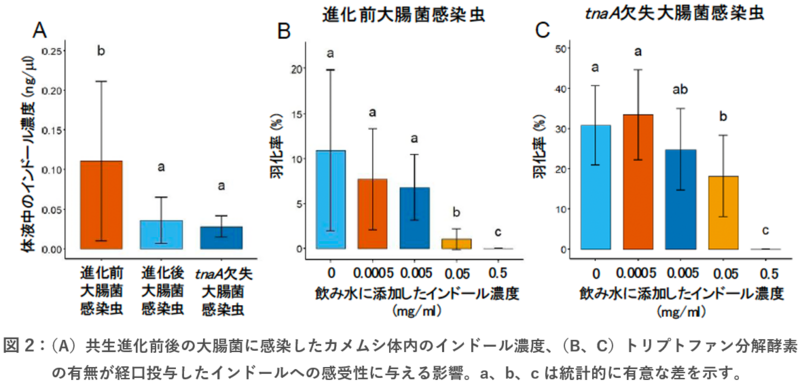
トリプトファン分解酵素はトリプトファンをピルビン酸、アンモニア、インドールに分解する反応を触媒します(概要図)。インドールには毒性があり、マウスやヒトでは腸内細菌のトリプトファン分解酵素によるインドールの産生により病気が引き起こされるという報告があります。共生進化前後の大腸菌を感染させたカメムシにおいて、体内インドール濃度を測定したところ、共生進化後の大腸菌を感染させたカメムシにおいてインドール濃度が有意に低下しており、トリプトファン分解酵素遺伝子を欠失させた大腸菌を感染させたカメムシでも同様にインドール濃度の低下が見られました(図2A)。試しに、進化前またはトリプトファン分解酵素遺伝子を欠失させた大腸菌を感染させたカメムシの幼虫にインドールを添加した飲み水を与えてみたところ、インドールの濃度が高くなるほど羽化率が低下しました(図2B、C)。さらに、トリプトファン分解酵素の欠失により羽化率の低下が緩和されました(図2B、C)。すなわち、トリプトファン分解酵素遺伝子の機能喪失により、毒性のあるインドールが産生されなくなることが、大腸菌の共生細菌化に関与している可能性が示唆されました。
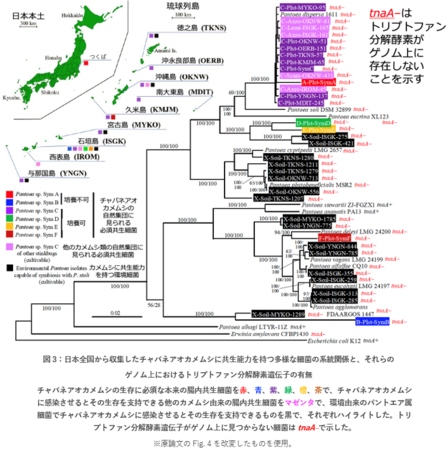
先行研究より、チャバネアオカメムシの日本集団では、その共生器官内にパントエア属(Pantoea)の6種の共生細菌のいずれかを保有することが知られています。他のカメムシ科やキンカメムシ科の多くの種も共生器官に近縁のパントエア属細菌を共生させています。さらに、カメムシ生息域の環境土壌中にはチャバネアオカメムシへの共生能力を持つパントエア属細菌の存在が報告されています(2016年1月11日 産総研プレス発表)。これら自然界で進化した、カメムシへの共生能力を持つ多様な細菌のゲノム配列を決定したところ、ことごとくトリプトファン分解酵素遺伝子を喪失していることが判明しました(図3)。
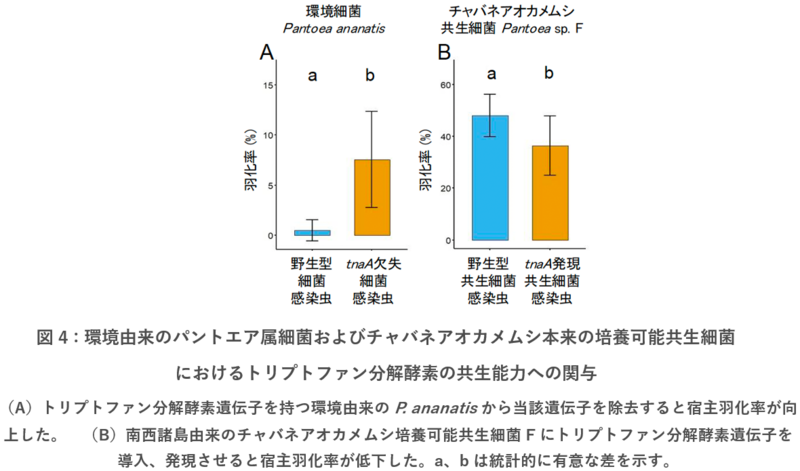
環境由来のパントエア属細菌の中でトリプトファン分解酵素遺伝子を持っているPantoea ananatisをカメムシに感染させたところ、まったく成虫が得られず、共生能力を持たないことがわかりました。一方、この細菌のトリプトファン分解酵素遺伝子を欠失させてからカメムシに感染させたところ、羽化成虫が得られるようになりました(図4A)。さらに、チャバネアオカメムシの南西諸島集団にみられる共生細菌F(Pantoea sp. F)にトリプトファン分解酵素遺伝子を導入して発現させたうえでカメムシに感染させたところ、羽化率が有意に低下しました(図4B)。すなわち、大腸菌のみならず多くのカメムシ共生細菌を擁するパントエア属細菌でも、トリプトファン分解酵素遺伝子の有無がカメムシへの共生能力に関わることが示されました。
これらの結果より、トリプトファン分解酵素というたった一つの酵素遺伝子の機能喪失もしくは抑制により、大腸菌がチャバネアオカメムシの生育を支える能力を持つ共生細菌になりうることが示されました。しかも、当該酵素遺伝子の喪失が自然界で進化してきた多様なカメムシ共生細菌で共通してみられたということで、実験室のみならず自然界でもトリプトファン分解酵素の喪失が、カメムシ類における腸内細菌との共生進化において重要な役割を果たしてきた可能性が明らかになりました。従来、宿主生物の生存に必須な共生細菌の進化というのは、そう簡単に起こるものではないと考えられていましたが、今回の成果に至る一連の研究により、共生進化が迅速かつ容易に起こり得ること、さらにその代謝的な基盤が実証的に示されました。研究室における進化実験と、野外生物集団の広範な調査を統合して、共生進化の分子機構の一端を具体的に解明した重要な研究成果です。
今後の予定
実際の自然界では、宿主側と共生細菌の双方にさまざまな変異が蓄積することによって共生進化が起こってきたと考えられており、今回明らかになったトリプトファン分解酵素の喪失というのは、それらのうち共生細菌側の変異の一つであると考えられます。その他にも存在すると予想される宿主側と共生細菌側の共生に関わる分子機構について、チャバネアオカメムシ-大腸菌実験共生進化系を駆使した実証研究と、野外カメムシ集団における多様な腸内共生細菌の比較解析を両輪として解明していく予定です。
共生の基盤となるいろいろな分子機構がわかってくると、関連遺伝子の導入、破壊、発現操作などによって、共生能力の賦与技術、共生関係のデザイン技術への展開も可能になると期待されます。このように「共生を創り出す」「共生をデザインする」試みにも取り組んでいきます。
大腸菌というのは元々、ヒトやマウスなど哺乳類の腸内細菌として単離されたものです。したがって、カメムシの共生細菌化した大腸菌を無菌マウスに感染させるなどの実験により、昆虫腸内共生と哺乳類腸内共生の相違点および共通点の探索にも取り組んでいく予定です。
論文情報
掲載誌:Nature Microbiology
論文タイトル:Tryptophanase disruption promotes insect-bacterium mutualism
著者:Yayun Wang†, Minoru Moriyama†, Ryuichi Koga†, Kohei Oguchi, Takahiro Hosokawa, Hiroki Takai, Shuji Shigenobu, Naruo Nikoh, Takema Fukatsu(†共筆頭著者)
DOI:10.1038/s41564-026-02264-z
用語解説
チャバネアオカメムシ-大腸菌実験共生進化系、昆虫-大腸菌実験共生進化系
チャバネアオカメムシは学名Plautia stali。半翅目カメムシ科に属する。ごく普通に見られる緑色のカメムシで、日本全国に分布する。さまざまな農作物を吸汁して害を与え、特にミカンなど果樹の重要害虫として知られる。大腸菌は学名Escherichia coli。環境細菌として、またヒトその他の哺乳類の腸内細菌として知られる。大部分の大腸菌は人畜に無害であるが、中にはO157 株のように強い病原性を示すものもある。分子生物学のモデル微生物として長年にわたり広く使われてきたため、研究が進んでいる。産総研では、チャバネアオカメムシに高速進化大腸菌を感染させて飼育維持することにより、実験室で迅速に共生進化を起こさせることに成功した。高速進化大腸菌とは、突然変異蓄積率が高くなるように遺伝学的に操作を加えることにより、分子進化速度を加速した大腸菌のことで、DNA ミスマッチ修復酵素遺伝子mutS を欠失させたΔmutS 系統の大腸菌を用いると、突然変異率が100倍程度に上昇し、分子進化速度も100倍程度に加速する。詳しくは2022年8月5日 産総研プレス発表を参照。
トリプトファン分解酵素
トリプトファンを分解してピルビン酸、アンモニア、インドールを生成する反応を触媒する酵素。tnaA遺伝子にコードされる。多くの細菌が持っているが、ほとんどの動物は持っていない。トリプトファンはヒトにおける必須アミノ酸のうちの一つで、側鎖にインドール環を持ち、芳香族アミノ酸に分類される。
共生細菌
宿主生物に共生している細菌のこと。存在部位は体表、腸内、体腔内、細胞内などさまざまであり、宿主への影響も有益なもの、有害なもの、どちらとも言い難いもの、環境条件によって変わるものなど、いろいろある。
必須アミノ酸
タンパク質を構成するアミノ酸のうち、動物の体内で十分な量を合成できず栄養分として摂取しなければならないアミノ酸のこと。ヒトではトリプトファンのほか、ロイシン、リシン、バリン、スレオニン、フェニルアラニン、メチオニン、イソロイシン、ヒスチジンが必須アミノ酸とされる。
インドール
ベンゼン環とピロール環が縮合した構造をとる有機化合物で、ヒト体内では腸内細菌によるトリプトファンの分解により生じる。悪臭および毒性があり、腸内で生成されるインドールはさまざまな疾患に関わることが報告されている。
共生器官
共生微生物を保有するために特殊化した宿主生物の器官のこと。カメムシの消化管後部には多数の盲嚢(もうのう)が発達し、その内腔に共生細菌を保有する。アブラムシなどで細胞内共生細菌を収容する菌細胞塊、ダイズなどで窒素固定細菌を保有する根粒なども共生器官の例である。
ピルビン酸
有機酸の一種で、生体内では主に解糖系における糖の酸化で生成され、いろいろな代謝で重要な役割を持つ。
パントエア属(Pantoea)
グラム陰性細菌に分類される細菌の属で、20種以上を含み、いろいろな環境より分離される。
プレスリリースURL
https://www.aist.go.jp/aist_j/press_release/pr2026/pr20260227/pr20260227.html